緊急通知:再次反轉!海關官宣:醫療物資出口無需實施產地檢驗!
2020-04-14 15:35:19
Landbridge平臺
周五經歷了一波三折的醫療物資出口商檢“大戰”,原以為會因為海關總屬發布的53號公告塵埃落定,沒想到又再次反轉。
讓我們來回顧一下此次醫療物資出口商檢變化過程:
4月10日凌晨00:01,海關系統更新,對19個商品編碼項下的醫療物資實施出口法檢。
4月10日早上8點,海關系統撤銷法檢要求。
4月10日中午12點,海關總署發布53號公告,對11個商品編碼下的醫療物資實施出口商品檢驗。
4月11日,海關發布緊急通知,對于53號公告的具體操做出了新的解釋。
不同于其他出口法檢商品,此次53號公告新增法檢出口醫療物資采取的是驗證管理方式,無需實施產地檢驗,報關時無需出口電子底賬,企業只需正常申報報關單。
醫療物資出口快速通關檢驗指南
根據海關總署2020年第53號公告,自4月10日起,對“6307900010”等海關商品編號項下的11類醫療物資實施出口商品檢驗,共涉及19個HS編碼。之前,對出口檢測試劑已實施衛生檢疫。
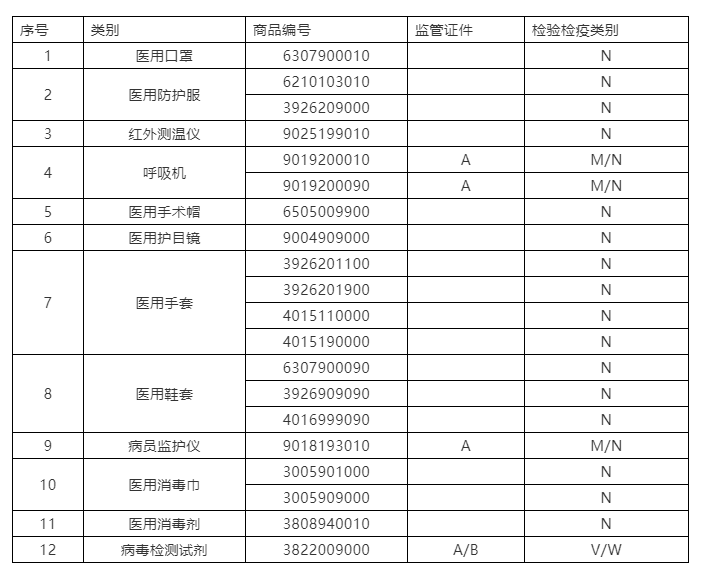
1、出口申報
對53號公告所列11類出口法檢醫療物資企業通過單一窗口申報報關,不同于其他出口法檢商品的是,此次新增法檢出口醫療物資一般無需實施產地檢驗,報關時無需出口電子底賬。
(1)對出口法檢醫療物資,企業需在報關單商品名稱欄填報用途,并注明是否醫用,檢測試劑需注明是否為新型冠狀病毒檢測用。
溫馨提示:
同一HS編碼下既有醫療物資又有非醫療物資的,應根據商品本身特征即生產制造標準,確定是否醫用。
(2)對三部委“5號公告”所列(含公告后續調整所列)的出口新型冠狀病毒檢測試劑、醫用口罩、醫用防護服、呼吸機、紅外體溫計5類醫療物資,企業向海關報關時,須提供書面或電子聲明和我國醫療器械產品注冊證書。新冠病毒檢測試劑還須提供藥監部門出具的出口銷售證明。
(3)對其他出口法檢醫療物資,企業向海關報關時,應當提供醫療器械產品注冊/備案證明和質量安全承諾聲明。對無相關證明和承諾聲明的,海關將實施嚴密監管。
(4)對新冠病毒檢測試劑,發貨人應當申請衛生檢疫審批,憑《入/出境特殊物品衛生檢疫審批單》通過單一窗口報檢,經海關檢驗合格后,獲得電子底賬,報關時填寫電子底賬帳號。
鄭重提示:
企業必須按規定如實向海關申報,對將醫用物資偽報為非醫用物資的,依法從重處罰;涉嫌構成犯罪的,移送地方公安機關追究刑事責任。
2、質量安全要求
出口法檢醫療物資應當符合進口國(地區)的要求,對進口國(地區)無質量安全標準要求的,應當符合我國質量安全標準。
小工具
醫療物資國內外質量安全標準可登陸“海關總署網站—總署概況—商品檢驗司—政策法規”欄目查詢(不定期更新),訪問地址:http://sjs.customs.gov.cn/sjs/zcfg56/index.html
部分國家(地區)防疫物資技術法規和標準要求(第三版),訪問地址:http://sjs.customs.gov.cn/sjs/zcfg56/2963129/index.html
我國和國外部分國家(地區)防疫醫療物資質量安全標準和主要項目(第一版),訪問地址:http://sjs.customs.gov.cn/sjs/zcfg56/2963129/index.html
3、裝運前檢驗
按照中國和國外政府簽訂的雙邊協議,對出口至部分國家和地區的商品需申請實施裝運前檢驗。

再次聲明:
企業是出口醫療物資質量安全第一責任人,海關依法實施檢驗監管。出口屬于摻雜摻假、以假充真、以次充好的商品或者以不合格進出口商品冒充合格進出口商品的,將依法依規嚴厲查處;構成犯罪的,依法追究刑事責任。
海關發布醫療物資出口快速通關檢驗指南
《海關實施出口醫療物資法定檢驗工作方案》的通知(署監發「2020」72號),內容摘要及解讀如下:
按照72號文件要求,對于53號公告規定的11類(19個商品編碼)出口法檢醫療物資,采取的是驗證管理方式,就是不需要做商品品質檢驗,無需出口電子底賬,企業正常申報報關單。
單證提交要求:在三部委發布的“5號公告”里的5類醫療物資,提交醫療器械產品注冊證和企業承諾聲明;在三部委發布的“5號公告”外的醫用物資,企業提交注冊證和質量安全承諾書,非醫用物資不要求提交注冊證和質量安全承諾書。
海關審核要求:三部委5號公告涉及5類醫療物資,而海關53號公告涉及11類醫療物資。其中,4類相同,7類不相同。但都是對于醫療物資的新措施,不是對于非醫療物資的新措施。所以,海關申報系統中并沒有對53號公告中的19個HS設置出口商檢監管條件。海關采取電子審核加人工審單的方法,處理53號文件涉及的申報單證。涉及53號公告的出口防疫物資申報時,不需要電子底賬,數據不走ECIQ系統。
三部委5號公告的4類商品按5號公告要求辦理,需提供中國醫療器械產品注冊證和企業承諾說明書,不需要做產品法定檢驗。對53號公告新增的7類商品,綜合業務崗位幾乎100%人工審單,發現未放行的可以聯系海關審單部門。
對非醫用的,若沒被布控,直接放行;對醫用的,需企業提供注冊證書(可以是電子掃描件)及出口企業的質量承諾書,有上傳的,原則上(被風險布控或者綜合業務崗人工審單有疑問的、決定布控除外)予以放行,沒有上述注冊證書或者出口企業質量保證承諾書的,將可能被布控。
查驗資料要求:如果產品涉及醫療物資,企業需提供注冊/備案證明和質量安全承諾書。對于現場無法判定或企業提出異議的送實驗室檢測。72號文中明確了“在確定是否為醫療物資時,應根據商品本身特征而非申報用途”。
部分國家(地區)防疫物資技術法規和標準要求
出口醫療物資需要符合國內出口標準,同樣也需要遵循國外的進口標準。

如何區分醫用和非醫用口罩
1、口罩的基本分類與細分
口罩從用途可以分為醫用/非醫用兩大類。顧名思義,醫用口罩主要用于醫療方面的防護,可以細分為醫用防護、醫用外科、一次性醫用三種;非醫用口罩也被稱為個人防護口罩,可根據其適用場景,可細分為防顆粒物和日常防護兩種。不同用途的口罩其技術要求不同、適用范圍也不同。
中國主要的口罩分類
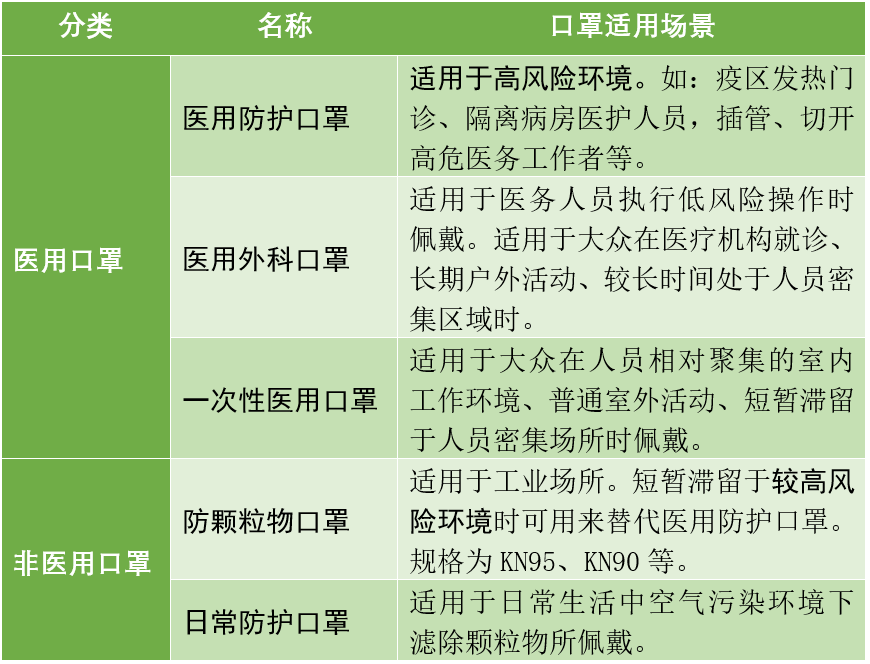
2、利用外觀與包裝信息區分醫用/非醫用口罩
通過口罩結構區分
通過過濾閥分辨。帶過濾閥的口罩一般不會是醫用口罩。如中國醫用防護口罩標準GB 19803-2010 第4.3條款就明確規定“口罩不應有呼氣閥”,這樣可避免飛沫、微生物等通過呼氣閥呼出,從而危害他人。而民用口罩允許有呼氣閥,通過呼氣閥可以減小呼氣阻力,從而有利于作業人員長時間工作。

通過外包裝上的信息分辨
正規途徑銷售的口罩產品的最小單元包裝上應該有商品名稱、執行的標準和防護等級等信息。這些商家明示的信息可以作為一個分辨點,如商品名稱中帶有“醫用”或英文“surgical”“Medical”等字樣的,一般可判定為醫用口罩。

3、適用標準區分醫用/非醫用口罩
醫用口罩在不同國家/地區適用不同的標準和認證要求,企業和個人可根據產品進口國家/地區,根據產品的適用標準進行區分,產品適用標準和認證信息可從產品外包裝或生產者提供的檢測報告或證書獲得。
出口美國
醫用口罩在美國屬于醫療器械,適用《醫用口罩材料性能標準規范》(ASTM F2100),由美國食品藥品監督管理局(FDA)管理,須通過501K注冊或近期FDA公布的其它途徑,獲得工廠注冊和醫療器械列名后方可在美國上市。因此,輸往美國的口罩外包裝或檢測報告或證書上有上述內容的,可被判定為醫用口罩。
出口美國非醫用口罩不屬2020年第5號公告范圍,但企業應注意,產品需通過NIOSH注冊方可在美國上市。

出口歐盟
歐盟醫用/非醫用口罩均需加貼CE標志,但適用標準不同。
醫用口罩在歐盟屬于I類器械,分為I類非無菌和無菌兩種,需按照歐盟醫療器械指令93/42/EEC(MDD)或歐盟醫療器械條例EU2017/745(MDR)加貼CE標志,對應的標準是EN14683,輸往歐盟的口罩外包裝或檢測報告、證書上有上述內容的,可被判定為醫用口罩。

需要注意的是,根據口罩無菌/非無菌狀態,歐盟采取不同的合格評定辦法,非無菌醫用口罩企業只需進行CE自我符合性聲明,不需要通過公告機構認證。在準備好相應文件及測試報告等資料后,即可自行完成符合性聲明。無菌醫用口罩還必須由授權公告機構進行CE認證。
出口歐盟非醫用口罩不屬于醫療器械,但需符合歐盟個人防護設備條例EU2016/425(PPE)要求,由授權公告機構進行CE認證并頒發證書,對應的標準是EN149。
出口其它國家和地區
輸往其它國家和地區口罩產品,可參考其提供的中國標準檢測證書與注冊備案信息進行判斷,中國醫用口罩標準有三個,GB 19083-2010、YY 0469-2011、YY/T 0969-2013,使用這三個標準生產的口罩可被判定為醫用口罩。
中、美、歐三個國家或地區醫用口罩標準

4、通過政府注冊管控信息進行區分
由于醫用口罩在大部分國家或地區都是按照醫療器械進行注冊或管控的,消費者可以進一步通過相關注冊管控信息進行分辨。下面以中、美、歐三個國家和地區舉例分析。
中國
醫用口罩在中國屬于二類醫療器械,是由省一級藥品監管部門實施注冊管理,可以通過醫療器械查詢醫療器械準入號進行查詢。鏈接為:
http://www.nmpa.gov.cn/WS04/CL2590/
美國
已獲得美國FDA準入的口罩產品可以通過其官網查詢注冊證書號進行查詢,鏈接為:
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfPMN/pmn.cfm
另外根據FDA最新政策,目前是在滿足一定條件的情況下認可中國標準的口罩,其授權企業的鏈接為:
https://www.fda.gov/media/136663/download
歐盟
出口歐盟醫用口罩可通過獲得授權的公告機構進行查詢,其中歐盟醫療器械指令93/42/EEC(MDD)授權的公告機構查詢地址為:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=13
歐盟醫療器械條例EU 2017/745(MDR)授權的公告機構查詢地址為:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=34。
(來源:騰道外貿大數據)
版權與免責聲明:此稿件為引述消息報道,稿件版權歸原作者所有,Landbridge平臺不對本稿件內容真實性負責。如發現政治性、事實性、技術性差錯和版權方面的問題及不良信息,請及時與我們聯系,并提供稿件的【糾錯信息】。糾錯熱線:0518-85806682

Landbridge平臺常務理事單位
- [常務理事單位] 沈陽陸橋國際貨運代理有限公司
- [常務理事單位] 湖南中南國際陸港有限公司
- [常務理事單位] 成都厚鯨集裝箱租賃有限公司
- [常務理事單位] 湖南德裕物流有限公司
- [常務理事單位] 安德龍國際物流集團
- [常務理事單位] 重慶逆鋒國際貨運代理有限公司
- [常務理事單位] 陜西遠韜供應鏈管理有限公司
- [常務理事單位] 天津海鐵聯捷集團有限公司
- [常務理事單位] LLC ST GROUP
- [常務理事單位] 宏圖集裝箱服務有限公司
- [常務理事單位] 哈薩克斯坦Falcon
- [常務理事單位] 青島和泰源集裝箱堆場
- [常務理事單位] 俄羅斯戰艦國際貨運代理有限公司
- [常務理事單位] 青島亞華集裝箱堆場
- [常務理事單位] 海晟(上海)供應鏈管理有限公司
- [常務理事單位] 俄羅斯西格瑪有限責任公司





